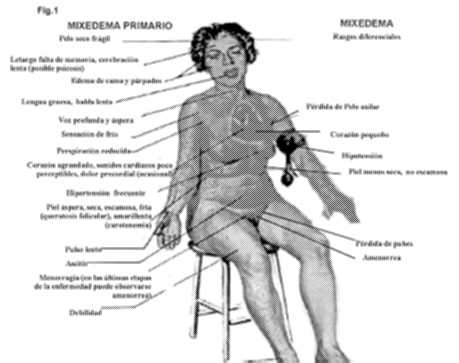
Fig.1
HIPOTIROIDISMO
Prof. Dr. Víctor José
Villanueva
El síndrome de
hipofunción tiroidea es bastante frecuente aunque muchas veces resulta
subdiagnosticado debido a su escasa expresividad clínica razón
por la cual el paciente no consulta o bien lo hace con algunos signos no
característicos que llevan al médico a pensar en otras patologías
como sucede en la ganancia de peso que equivocadamente diagnostica obesidad
o por la apatía, astenia, hiporexia, inmovilidad (no quieren levantarse
de la cama) y torpeza mental evocan una demencia o una depresión.
Se calcula que afecta alrededor del 10% de la población anciana
en los países del hemisferio norte, y de este porcentaje, alrededor
del 7% son mujeres.
Etiopatogenia :
Teniendo en cuenta
las causas y mecanismos por las que se puede llegar al fallo tiroideo es
posible clasificarlo en tres categorías:
1- Hipotiroidismo primario:
Producido porenfermedades
propias de la glándula tiroides que destruyen los folículos
tiroideos.
La histopatología
evidencia lesiones variadas con reemplazo de los folículos por inflamación,
esclerosis u otras. Cursa con elevación de la tirotrofina hipofisaria
por liberación del freno ejercido por la tiroxina y la triiodotironina
que están disminuidas o ausentes. La tiroides puede afectarse por
diferentes causas:
3- Hipotiroidismo terciario:
La adenohipófisis
y la tiroides son sanas pero sufren las consecuencias de enfermedades del
hipotálamo que resulta anulado y no produce hormona liberadora de
tirotrofina. Este hecho altera el sistema de retroalimentación glandular
con el consiguiente déficit de tirotrofina que a su vez lleva al
déficit de hormonas tiroideas. Es decir que hay carencia de TRH,
TSH, T3 y T4. La estimulación del sistema con TRH restablece la
normalidad. Lo mismo se puede lograr con TSH para la secreción tiroidea.
El estudio histológico muestra destrucción del hipotálamo
con atrofia de la hipófisis y tiroides. El mismo tipo de enfermedades
y lesiones que atacan la hipófisis pueden hacerlo con el hipotálamo.
Primario
Hipotiroidismo : Secundario
Terciario
Sintomatología:
Hipotiroidismo primario:
Es la variedad más
frecuente de todas. Fue descrito por Gull en 1873 con el nombre de mixedema
por este signo cutáneo muy llamativo. Su causa más frecuente
en la actualidad es la tiroiditis atrófica autoinmune. Anteriormente,
la causa más frecuente era la carencia de yodo en el agua y los
alimentos pero en virtud de la profilaxis de la carencia yódica
con el agregado de este metaloide en la fabricación de la sal de
cocina esta etiología cedió el primer lugar. En segundo término
siguen las alteraciones de la síntesis hormonal, por alteraciones
enzimáticas (variedad no endémica del hipotiroidismo), luego
sigue en orden de frecuencia el hipotiroidismo por carencia yódica
o sustancias bociógenas en la dieta en las zonas endémicas.
El aspecto general
del hipotiroideo primario es de un individuo, generalmente mujer, obeso
(falsa obesidad pues el aumento de peso se debe al mixedema), con tinte
pálido amarillentode la piel y mucosas (el mixedema separa los vasos
dérmicos de la superficie cutánea, hay vasoconstricción
de los mismos y por falta de utilización de los carotenos de la
dieta para la síntesis de vitamina A se acumulan en la sangre).
Es apático e indiferente, con cara redondeada y ojos entrecerrados
por el mixedema palpebral que comunica aspecto somnoliento y cierta expresión
de estupidez. El paciente es friolento y se abriga en exceso, aun en verano.
Por la falta de hormonas
no se metaboliza los mucopolisacáridos proteicos de la sustancia
fundamental del tejido conjuntivo de la piel y otros órganos. Dicho
compuesto atrae agua y sodio del compartimento vascular y esta mezcla glucoproteica
con agua y sodio produce el mixedema. Este se presenta como una infiltración
que "hincha" la piel pero como es elástico, luego de ser comprimido
por el dedo no deja la fovea como el edema común. Se lo ve donde
existe abundante tejido celular subcutáneo laxo como los párpados,
dorso de la manos y pies, parte superior del dorso e inferior de la nuca.
El mixedema de la lengua lleva a la macroglosia y esta lengua grande queda
comprimida contra las arcadas dentarias con lo que se imprime la marca
de los molares o incisivos en sus bordes. El mixedema de las cuerdas vocales
junto con el de la lengua comunica a la voz un tono áspero y grueso.
Hay otras alteraciones en la piel y faneras como la frialdad (por el hipometabolismo
y la vasoconstricción), sequedad (hiposecreción sudoral y
sebácea) y aspereza (descamación e hiperqueratosis perifolicular).
El pelo y vello corporal se vuelven secos y quebradizos con caída
pero no hay alopecia porque queda un corto tallo sobresaliendo del folículo.
El hipometabolismo
e infiltración del sistema nervioso central origina disminución
de la actividad mental con bradipsiquia, astenia, torpeza mental, somnolencia,
indiferencia; el paciente no solo puede simular un cuadro de demencia o
depresión sino que muchas veces lo padece.
El mixedema e hipoactividad
del músculo esquelético ocasiona hipo y bradiquinesia con
escasa tendencia a la actividad física, el paciente pasa todo el
día en cama o sentado y se duerme con frecuencia. El pellizco de
un músculo superficial (como el bícep) muestra un rodete
miotónico evidente y de gran duración (10 segundos o más)
en lugar de uno pequeño pero que no dura más de 2 o 3 segundos.
Es típico que el reflejo aquiliano o rotuliano sea lento (la contracción
muscular es normal pero la relajación es lenta).
Las mismas alteraciones
en el miocardio ocasionan bradifigmia con cardiomegalia, a lo que suele
agregarse un derrame pericárdico.
Estas alteraciones
más la eventual hipertensión arterial por la vasoconstricción
pueden llevar a la insuficiencia cardíaca.
En hipotiroidismos
severos puede verificarse hidrotórax y ascitis además del
derrame pericárdico.
La hipomotilidad de
la fibra muscular lisa digestiva junto con la hiposecreción de sus
glándulas produce costipación.
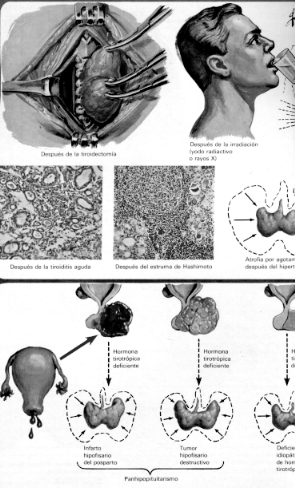
En el cuello se puede
encontrar bocio en los casos en los casos de alteraciones de la hormonogénesis
y en las tiroiditis inmunitarias en periodo de actividad pero que desaparece
o se reduce cuando llega a la fibrosis. En los casos de hipotiroidismo
postoperatorio se verá la cicatriz cervical correspondiente. En
los casos de terapia radiante del cuello, en los primeros meses se verá
eritema difuso y luego melanodermia.
Hipotiroidismo secundario:
A este cuadro de fallo
tiroideo se agrega manifestaciones de insuficiencia adenohipofisaria global
pues raramente sus enfermedades afectan selectivamente la secreción
de tirotrofina y por ello se verificará manifestaciones de falla
de gonadotrofinas y corticotrofina. El problema en el anciano es que los
efectores de las gonadotrofinas ya no responden (testículos y ovarios)
razón por la cual no se verá sintomatología de esta
esfera. En cuanto a la insuficiencia suprarrenal secundaria habrá
marcada astenia, hipotensión ortostática, síntomas
de hipoglucemia y crisis de shock e hipoglucemia en cualquier situación
de alarma. Habrá pérdida total del vello corporal y anorexia
con desnutrición. La piel es blanco pálida, no amarillenta,
sin hiperqueratosis, es decir suave ( por falta de androcorticoides). El
mixedema en sus diversas localizaciones es menos marcado que en los casos
primarios. Si existe patología tumoral con crecimiento hacia arriba,
al cerebro, se comprimirá la vía óptica (quiasma)
con producción de hemianopsia heterónima (pérdida
de las mitades de los campos visuales de lados opuestos) y signos de hipertensión
intracraneal (cefalea, vómitos y edema de papilas ópticas).
Una causa frecuente
de insuficiencia hipofisaria en la mujer es el síndrome de Sheehan
o necrosis hipofisaria postparto en que el mismo se complicó con
shock hemorrágico que ocasionó la isquemia hipofisaria. El
paciente con este tipo de hipotiroidismo se caracteriza porque luego del
accidente no pudo desarrollar la lactancia (por falta de prolactina), quedó
con amenorrea definitiva y sufrió atrofia de la mama y genitales
externos (por falta de estrógenos debido a la anulación de
gonadotrofinas FSH y LH).
Hipotiroidismo terciario:
El enfermo agregará
manifestaciones hipotalámicas, neurológicas focales e hipertensión
intracraneal a las tiroideas e hipofisarias. Así, tendremos diabetes
insípida (poliuria de más de 5 litros por día con
hipostenuria: orinas con densidad 1,005 o menor en lugar 1,015 o más
como sucede en el normal, y polidipsia intensa). Secreción exagerada
de hormona antidiurética (cefalea, cambios de carácter, anorexia
y náuseas, convulsiones, edema de papilas ópticas). Hiperfagia,
trastornos del sueño, hiperglucemia, obesidad, hipertermia.
Laboratorio:
Existe algunos datos,
que si bien no son exclusivos de este síndrome ayudan en la sospecha
diagnóstica. Ellos son:
Anemia: la falta de hormonas
tiroideas suprime un estímulo para la eritropoyesis. La anemia será
normocítica normocrónica. En oportunidades será microcítica.
En los hipotiroidismos autoinmunes, especialmente en el Hashimoto, hay
también inmunidad contra las células parietales gástricas
con la consiguiente falta de secreción del factor intrínseco
que permite la absorción intestinal de la vitamina B12 lo que conducirá
a la anemia perniciosa (anemia macrocítica).
Glucemia: hay enlentecimiento
de la absorción intestinal de la glucosa lo que puede llevar a hipoglucemias
y curvas planas de tolerancia a la glucosa. En la variedad secundaria la
hipoglucemia en ayunas es constante y severa, con manifestaciones clínicas
por la falta de cortisol secundaria a la de ACTH.
Lípidos sanguíneos:
hipercolesterolemia
e hipertrigliceridemia. Suero sanguíneo con aspecto lechoso en ayunas
en la variedad primaria. En la secundaria por el déficit de cortisol
y desnutrición hay hipocolesterolemia.
Enzimas musculares: por
el mixedema intersticial e intrafibrilar con fragmentación de las
miofibrillas se puede encontrar elevación de la GOT, CPK y LDH.
Análisis específicos de
hipotiroidismo:
El dosaje de tiroxina
y de tirotrofina son fundamentales para el diagnóstico de hipotiroidismo
y para diferenciar si éste es primario o secundario. La determinación
de la triiodotironina no aporta mejores datos que las dos anteriores sino
que puede llevar a confusión pues a veces sus niveles no coinciden
con ellos. Por otra parte, más de las dos tercios de la T3 no provienen
de la glándula tiroides sino de la conversión periférica
de la T4 no siendo un índice fiel de su función y dependiendo
de otros factores como la actividad de las desyodinasas periféricas.
Por estas razones sus determinación es prescindible. La tiroxina
en sangre es de 4,5 a 12 microgramos por ciento y este nivel disminuye
en todos los tipos de hipotiroidismo. Como la tiroxinemia depende de la
cantidad de proteínas plasmáticas fijadoras de tiroxina,
en caso de sospecharse un déficit de ellas (desnutrición,
síndrome nefrótico, hepatopatías), se debe cuantificar
los niveles de tiroxina libre (el 0.03% de la que produce la glándula
y que es la metabólicamente activa) para evitar un falso diagnóstico
de hipotiroidismo. Sus valores oscilan entre 0,8 y 2,8 nanogramos por ciento
de plasma. La tirotrofina oscila entre 0,5 y 6 microunidades internacionales
por ml. En el hipotiroidismo primario, al suprimirse el mecanismo de retroalimentación
negativa de la hipófisis, asciende a cifras superiores a las 10
microunidades. En los hipotiroidismos secundario y terciario baja a menos
de 0,20 o no se la detecta en la sangre.
¿Cómo
diferenciamos el hipotiroidismo secundario del terciario?. Utilizamos la
prueba de la TRH-TSH basados en el siguiente razonamiento: en el hipotiropidismo
terciario existe lesiones hipotalámicas que anulan la secreción
de hormona liberadora de tirotrofina razón por la cual la adenohipófisis
deja de producir tirotrofina pero como solo está hipotrófica
y aun es capaz de responder al estímulo trófico, al inyectarse
la TRH por vía intravenosa, los niveles basales que estaban en cero
o menores que 0,20 microunidades, se elevan a más del 100%. En el
hipotiroidismo secundario existe lesiones hipofisarias que anulan las células
secretoras de TSH, el hipotálamo es normal y funcionante pero no
hay respuesta de TSH por falta de células efectoras de modo que
si se inyecta la TRH no se producirá modificación de los
valores bajos o nulos de la tirotrofina. Debemos recordar que en el hipotiroidismo
primario, la hipófisis se encuentra liberada del freno tiroideo
de modo que su estimulación con TRH producirá un aumento
aun mayor de los valores de TSH basales, es decir que habrá una
hiperrespuesta, superior a la que se verifica en la variedad hipotalámica.
El dosaje de gonadotrofinas da valores bajos en la variedad secundaria
y normales o altos en la primaria.
Prueba de la descarga
de yodo radiactivo con perclorato o tiocianato de potasio: sirve para explorar
la capacidad de la glándula para utilizar el yodo alimentario para
la síntesis hormonal para lo cual debe captarlo, reducirlo a ión
metálico y organificarlo (incorporarlo al aminoácido tirosina).
La organificación es un paso crucial sin el cual no hay producción
hormonal. El perclorato o el tiocianato tienen la capacidad de desplazar
el yodo no organificado de la célula folicular. Si se determina
la captación del I 131 y a continuación se administra oralmente
1 g. de cualquiera de estos dos compuesto orgánicos y una hora después
se vuelve a determinar la captación del isótopo, se verá
que en el paciente eutiroideo no hay desplazamiento del mismo desde la
glándula lo que se evidencia porque la radiactividad del plasma
sigue disminuyendo debido a que continua la captación del mismo.
En algunas formas de hipotiroidismo (bocios por trastornos de la síntesis
hormonal por alteraciones enzimáticas o bocios por enfermedades
autoinmunes) existe un fallo de la incorporación del metaloide a
la tirosina de modo que la administración de los aniones orgánicos
desplazan el yodo radiactivo captado por la glándula de su interior
y la radiactividad del plasma en lugar de disminuir porque se debiera seguir
captando el isótopo, aumenta por su expulsión desde el folículo.
La serología
es útil en el diagnóstico de la tiroiditis autoinmune atrófica
y en la linfocitaria crónica. Dosa los niveles de anticuerpos antitiroglobulina
y los microsomas de células tiroideas (estos últimos actuan
contra la enzima peroxidasa de los microsomas). Normalmente no los hay
o existen en muy baja cantidad (diluciones del suero sanguíneo menores
a 1/ 100). En el Hashimoto hay niveles de ambos a títulos por encima
de 1 / 1.000. En la variedad atrófica pueden estar elevados los
antimicrosomales solamente o ambos pero los antitiroglobulina no llegan
a valores mayores de 1 / 300.
Otros estudios:
Los estudios radiactivos,
salvo en el caso anterior ( hipotiroiodismo por defectos de organificación,
u otros especiales), no son de utilidad debido a la casi superposición
de los valores mínimos normales con los anormales por descenso.
Diagnóstico por imágenes:
En
los hipotiroidismos secundario y terciario la Rx. del cráneo y la
TAC o la RNM son útiles para estudiar los agrandamientos hipofisarios
o hipotalámicos por tumores o su reemplazo por inflamación
o necrosis.
La punción biopsia
de la tiroides con aguja fina (PAF) es útil para diagnosticar las
formas autoinmunes pero pueden ser reemplazadas ventajosamente por los
estudios de laboratorio que, además, no son cruentos.
Diagnóstico diferencial:
La infiltración
palpebral y de otras zonas junto con la palidez amarillenta y aspereza
al tacto pueden confundir con un síndrome nefrótico con insuficiencia
renal crónica (glomerulopatía). Más aun si se verifica
hipertensión arterial e hipercolesterolemia. En general en el hipotiroidismo
los valores de urea y creatinina son normales o bajos debido a la disminución
del catabolismo. No hay antecedentes de enfermedad renal. El examen de
fondo de ojo no muestra hemorragias ni exudados y las arterias podrán
estar estrechadas pero nunca en hilos de plata por no ser intensa la esclerosis.
Los dosajes hormonales aclaran el diagnóstico.
La signosintomatología
cognitiva y afectiva pueden simular una demencia degenerativa (Alzheimer)
o vascular o una depresión. En general estos cuadros cursan con
desnutrición y atrofia muscula, puede haber edema por hipoproteinemia
debido a falta de ingesta alimentaria pero no mixedema y la colesterolemia
suele estar disminuida. El laboratorio hormonal es definitivo.
Las anemias graves
con o sin desnutrición como la anemia perniciosa o las parasitarias
en los desnutridos, se manifiestan por palidez amarillenta con marcado
edema por hipoalbuminemia además que en ocasiones el fallo tiroideo
se manifiesta por una anemia macrocítica o microcítica en
lugar de normocítica. La existencia de signos de los cordones medulares
o el hallazgo de parásitos adultos, sus larvas o huevos junto con
las determinaciones de hormonas diferencian los cuadros.
Síndrome de resistencia periférica
a las hormonas tiroideas:
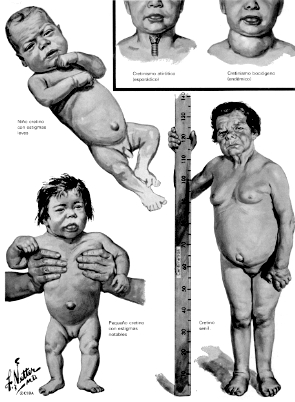
En 1967 se describió,
en niños, un cuadro clínico caracterizado por un síndrome
hipotiroideo con bocio difuso, TSH, T3 y T4 elevados. Es decir sintomatología
clínica de hipotiroidismo con signología de laboratorio de
hipertiroidismo. Además se halló numerosas malformaciones
o defectos congénitos (sordomudez, deformaciones de las epífisis
óseas con defectos del crecimiento y deformaciones de los miembros).
Se comprobó que existía resistencia de los receptores de
membrana nuclear de T3 y T4 con defecto del ingreso de ellas a los núcleos
celulares. Ello explica la sintomatología hipotiroidea con hipersecreción
de TSH que a su vez estimula la producción de T3 y la T4. Es un
síndrome raro del cual se ha descrito solo 60 casos hasta el presente.
Hipotiroidismo subclínico:
Existe ciertos pacientes
asintomáticos u oligosintomáticos pero con manifestaciones
inespecíficas para hipotiroidismo como cierta ganancia del peso
corporal, piel algo pálida y fría o seca, o con cierta astenia
y laxitud, costipación, algo de hipersensibilidad al frío
y en los cuales las mediciones hormonales dan valores normales de tiroxina
libre y de triiodotinina pero con niveles de TSH altos. Ello significa
que la función tiroidea está disminuida pero compensada por
una sobreestimulación hipofisaria que es suficiente para mantener
valores de T3 y T4 cerca de lo normal con un estado metabólico normal.
Esta situación se podrá mantener o virar a un hipotiroidismo
franco. El caso se suele verificar en la enfermedad de Hashimoto, la enfermedad
de Basedow sometida a cirugía o yodo radiactivo u otras enfermedades
autoinmunes como la diabetes tipo I, vitiligo y cirrosis biliar primaria.
Es útil efectuar una prueba de la TSH-TRH que, como la adenohipófisis
está liberda de la tiroides, dará una respuesta exagerada
de la TSH.
Síndrome del enfermo eutiroideo:
Una parte de la tiroxina
(con cuatro átomos de yodo), el 33%, sufre una desyodación
en la posición 5 (anillo externo) transformándose en triiodotironina
(tres átomos de yodo) a nivel de la mitrocondrias celulares rtisulares
por desyodinasas y este compuesto es el que ejerce la acción hormonal.
Otro porcentaje, 40%, por la mismas enzimas pierde un átomo de yodo
en la posición 3 (anillo interno) originando la T3 reversa o inversa
(rT3) que es inactiva y no ejerce acción alguna. Ambas moléculas
prosiguen su metabolismo intracelular al continuar perdiendo el metaloide
halogenado originando la diiodo y monoiodotirosina para luego liberar yodo
y tirosina. Todos ellos vuelven a la sangre y son reutilizados por los
folículos glandulares para nueva síntesis hormonal.
En diversas circunstancias
clínicas se produce una modificación de estos procesos del
metabolismo hormonal que se caracterizan por disminución de los
niveles séricos de T3, aumento de los de rT3, normalidad o leve
disminución de la T4 y sin modificación de la TSH, todo ello
con una situación metabólica de normotiroidismo. En esto
consiste el síndrome del enfermo eutiroiodeo. Las enfermedades en
las que se verifica esta anomalía `son graves, agudas o crónicas
como hepatopatías o nefropatías con fallo parenquimatoso,
infarto de miocardio, diabetes mellitus descompensada, sepsis, procesos
febriles no infecciosos graves, desnutrición calórico proteica,
ayuno prolongado, traumatismos extensos, cirugía amplia, fármacos
(propranolol, amiodarona, dexametasona).
Se cree que la inhibición
de la 5 desiodinasa en el hígado y riñón, normalmente
responsable de los niveles de T3 circulante, originaria la hipotriiodotironinemia
y como ella se encarga también de la desyodación de la rT3,
su menor actividad originaría la elevación de esta última.
Otros afirman que existe una captación hepática y renal reducidas
para tiroxina con lo que hay poco substrato para la conversión a
T3. Algunos afirman que en esta situaciones existe inhibidores plasmáticos
de unión de T4 a las proteínas transportadoras con lo que
habría transporte insuficiente de ella al hígado y riñones.
Además de la
disminución de los valores plasmáticos de T3 y elevación
de los de rT3, la T4 total puede estar normal con ligera elevación
de T4 libre, T4 total baja pero fracción libre normal y T4 total
alta con leve elevación de la libre. Los paciente con T4 total baja
pueden simular un hipotiroidismo pero al determinar la fracción
libre se observa su normalidad. En caso de que ésta también
descienda se medirá la TSH que estará normal y la rT3 que
también será normal o alta. En caso de hipotiroidismo la
TSH estará elevada y la rT3 disminuida. En los casos de T4 total
y libre altas la medición de T3 libre y rT3 dan valores bajos o
normales.
Se interpreta que estas
variaciones de los valores hormonales sanguíneos con función
tiroidea suficiente son intentos del organismo para disminuir las oxidaciones
tisulares en situaciones de emergencia en las que las necesidades energéticas
deben emplearse para otros fines o en determinados órganos en detrimento
de otros que para ese momento no son esenciales. Por estas causas no se
tratan dichos síndromes en lo que se refiere a las variaciones de
los valores plasmáticos de las hormonas tiroideas.
Coma hipotiroideo:
Es un cuadro grave
con alta mortalidad a pesar de los adelantos farmacológicos con
la síntesis de las hormonas tiroideas por la industria farmacéutica
y la disponibilidad de la asistencia respiratoria mecánica para
la administración del oxígeno.
Se instala en un paciente
con severa insuficiencia hormonal desencadenado por factores como infecciones,
exposición al frío, traumatismos, cirugía, uso de
tranquilizantes u otros depresores del sistema nervioso, enfermedades respiratorias
o de otro tipo que alteran la ventilación pulmonar.
Se caracteriza por
un coma de grado variable con depresión de la respiración,
bradicardia, hipotensión arterial, hipotermia (menos de 35º
rectal), hiporreflexia o arreflexia osteotendinosa. En los casos de hipotiroidismo
primario la piel está seca, gruesa y áspera conservando algo
del vello corporal, en el secundario es fina, suave, con arrugas y sin
vello corporal.
El laboratorio muestra
hipoxemia con hipercapnia y acidosis respiratoria, hiponatremia dilucional,
hipoglucemia (especialmente en el hipotiroidismo secundario). El dato importante
es la disminución de los valores de T4 y T3 totales y libres. Estas
determinaciones tardan algunos días en efectuarse razón por
la cual, una vez extraída la sangre para su realización debe
iniciarse el tratamiento.
Crisis hipertiroidea:
A pesar de que en este
ejemplar de nuestra revista nos ocupamos del hipotiroidismo haremos referencia
a este cuadro hipertiroideo por no haberlo tratado en el volumen anterior
que se refería a los hipertiroidismos.
Es una complicación
propia de la enfermedad de Graves Basedow que no se ve en las otras formas
de hiperfunción tiroidea. Se le denomina, también, crisis
tirotóxica, y, por lo aparatoso de sus manifestaciones se le llama
tormenta tiroidea. Es un cuadro grave con una mortalidad del 20% aunque
afortunadamente se lo ve poco en la actualidad gracias a la selección
de los pacientes que van a ser operado del Graves, a la mejor preparación
llevándolos a la cirugía eutiroideos o por lo menos betabloqueados.
Antiguamente la causa principal era la tiroidectomía en pacientes
aun hipertiroideos por falta de drogas antitiroideas, en menor proporción
los que se trataban con yodo radiactivo también sin estar normotiroideos.
Actualmente los casos que aparecen lo hacen en pacientes no tratados o
deficientemente tratados que sufren un stress (infección, traumatismo,
cirugía no tiroidea, deshidratación, etc.). El cuadro se
produce por liberación de grandes cantidades de T3 y T4 y por la
gran estimulación simpática en un paciente que ya tiene aumentados
los receptores beta adrenérgicos. La sintomatología se instala
bruscamente y consiste en ansiedad, temblor fino distal, inquietud, sudoración
caliente, taquicardia u otra taquiarritmia, diarrea, confusión mental,
fiebre, postración progresiva y coma. Hay marcada atrofia muscular
con debilidad de las contracciones con rápido agotamiento.
El diagnóstico
se sospecha en el contexto de un paciente con sintomatología hipertiroidea
que sufre una intercurrencia aguda y se establece con el hallazgo de valores
altos de T4 y bajos o ausencia de TSH en la sangre. Con la sospecha clínica,
sin esperar el resultado del análisis hormonal, debido a lo grave
del cuadro, se debe iniciar el tratamiento. Se debe frenar la secreción
tiroidea con los antitiroideos conocidos, preferentemente el propiltiouracilo
que, además, inhibe la transformación de T4 en T3, desafortunadamente
el exceso de hormonas secretados y liberados no pueden ser influenciados
por esta medicación y además no se dispone del mismo en nuestro
país, solo hay metimazol que se administra a la dosis de 20 mg.
por vía oral cada 4 a 6 hs. También se puede dar yodo por
vía oral: 10 gotas c/8 hs. o i.v. 1 g.c/ 8 hs, este elemento actúa
por efecto de Wolf-Chaicoff que inhibe la captación y organificación
del yodo iónico lo que frena la producción hormonal. Algunos
autores aconsejan iniciarlo varias hs. después de comenzar con el
antitiroideo para que no sea utilizado en la síntesis hormonal hasta
que ejerza su acción. El efecto periférico hormonal, en cierto
modo de tipo estimulación simpática, se puede antagonizar
con propranolol, 40 a 80 mg. por boca cada 6 hs, si es preciso, por vía
i.v. a razón de 1 mg. por minuto en goteo rápido hasta totalizar
10 mg. Se debe usar hidrocortisona: 100 mg. i.v. c / 6 hs. porque inhibe
la conversión de T4 a T3, además baja la fiebre y mantiene
el volumen intravascular. Se debe combatir la fiebre con compresas frías
en las axilas, zonas inguinales y partes laterales del cuello. Se debe
reponer la volemia con soluciones glucosalinas. Si se sospecha que la infección
desencadenó el proceso, se debe administrar antibióticos.
Toda esta terapéutica requiere internación en una unidad
de cuidados intensivos.
Tratamiento:
El tratamiento del
hipotiroidismo en sus tres formas etiopatogénicas consiste en la
sustitución de la secreción glandular insuficiente con hormonas
tiroideas exógenas naturales o sintetizadas por la industria farmacológica.
No se utiliza la estimulación glandular con TSH o TRH por ser muy
caras y por crear resistencia por anticuerpos luego de un tiempo de su
aplicación o determinar fenómenos de hipersensibilidad.
Antiguamente se utilizaba
extracto de glándula tiroides de cerdo o tiroglobulina del mismo
origen que contienen T3 y T4 aunque no en la proporción en que las
produce la glándula humana creando problemas de dosificación.
Con la síntesis de tiroxina y de triiodotironina artificiales en
la industria se solucionó estos problemas. La tiroxina actúa
en forma lenta, comienza a las 48 hs. y llega a su máximo en 7-8
días para agotar su efecto en 30 días. La triiodotironina
comienza a actuar a las 6 hs. y llega al máximo a las 48 agotándose
a la semana. De estas características surge que para el tratamiento
de un hipotiroidismo establecido crónico es suficiente con la tiroxina
mientras que para un coma hipotiroideo está indicada la triiodotironina.
En cuanto a las dosis debe considerarse que la producción diaria
de T4 es de alrededor de 100 microgramos y la T3 de 25. También
debe tenerse en cuenta la situación clínica del paciente
y la etiología del hipotiroidismo. En cuanto a la situación
clínica debe considerarse que en el anciano frecuentemente existe
ateroesclerosis coronaria y que en cierta forma el hipometabolismo del
déficit glandular lo protege de la agravación de la cardiopatía
isquémica por lo que el tratamiento debe iniciarse con dosis bajas
y aumentarlas muy lentamente hasta llegar al eutiroidismo sin por ello
llevar una cardiopatía hasta entonces asintomática a etapa
sintomática descompensada. Lo mismo para la insuficiencia cardíaca
y las arritmias. En todo caso, si el eutitroidismo significa aparición
de angor o su rebeldía al tratamiento es preferible dejar al paciente
con cierto grado de hipotiroidismo. En el caso de hipotiroidismo secundario,
es conveniente, antes de iniciar la administración de hormona tiroidea,
administrar cortisol unos pocos días previamente para evitar que
se desencadene una crisis suprarrenal. En el hipotiroideo crónico,
estable, sin cardiopatía, se inicia el tratamiento con 50 microgramos
diarios de tiroxina en una sola toma controlándolo cada 10 días
y aumentando la dosis en 25 microgramos hasta llegar a 150 o 175,a veces
200 como dosis diaria. La tiroxina viene en comprimidos con 25-50 y 100
microgramos de la droga (Levotiroxina de Laboratorios Glaxo). También
existe el preparado T4 de Laboratorios Montpellier en que un comprimido
con 100 ug. está dividido en cuatro porciones con 25 c / u. Los
parámetros a controlar son el peso , frecuencia del pulso y concentración
del colesterol y CPK en sangre. Luego del mes de iniciado el tratamiento
se solicita un dosaje de TSH y T4 en plasma para ajustar la dosis. En caso
de antecedentes de infarto de miocardio, angina de pecho, arritmias o insuficiencia
cardíaca, se debe comenzar con 12,5 ug. de la hormona modificándola
cada quince días en la misma proporción y no pasando de 75
a 100 ug. de dosis total diaria. No tiene objeto utilizar triodotironina
pues su corta acción exige varias tomas diarias lo cual expone al
olvido de tomas e incomodidad que llevan al abandono del tratamiento. Algunas
personas prefieren utilizar un preparado con T3 y T4 para conseguir un
efecto que al comenzar rápido, se mantenga todo el día con
una sola toma pero no supera a la tiroxina sola en sus efectos beneficiosos
y es más cara porque tiene las dos hormonas en el comprimido. Además,
vuelve más difícil la dosificación de cada una de
ellas. El preparado existente es el Levotrin (Glaxo) que tiene 10 ug. de
T3 y 90 de T4. La dosis es de 1- 2 comprimidos diarios.
Un paciente bien tratado
es aquel que tiene un peso acorde a la talla, pulso entre 60 y 100 x ,
colesterol y CPK normales, T4 entre 4 y 10 ug % y TSH entre 0,5 y 5 uUI/ml.
En el coma mixedematoso
el tratamiento de elección es la triiodotironina por vía
intravenosa lo cual es imposible en nuestro país por no contarse
con preparados inyectables de manera que se utiliza esta hormona administrándola
por sonda nasogástrica. La dosis es de 12,5 ug. cada 6-8 hs. El
preparado comercial es Tri-ioido-tironina Glaxo con 10 y 20 ug. de la droga.
El paciente debe ser internado en Terapia Intensiva, abrigado para combatir
la hipotermia, antes de iniciar la hormona tiroidea inyectar 100 mg. de
hidrocortisona i.v. y seguir con la misma dosis y vía c/8 hs. No
darle más de 1000 a 1500 ml. de agua i.v. por día por la
hipoosmolaridad plasmática. Darle sodio y glucosa hipertónicos
para restablecer la tonicidad plasmática y combatir la hipoglucemia.
Si hay hipovolemia indicar dextran o albúmina humana. Si hay signos
de infección indicar antibióticos de amplio espectro como
cefalosporinas de tercera generación hasta aislar el germen. Cuando
el paciente sale del coma darle T3 y T4 juntas(Levotrin 1 comp. por día
más Triiodo tironina de 25 mg. 1 comprimido diario)durante 7 días
y luego continuar con T4 sola 100 ug. por día que se irá
ajustando periódicamente como en un caso crónico.

Fig.1
| PBO y BEI: bajos; no aumentan después de TSH | Bajos, pero aumentan después del TSH |
| I133 :captación de 24 horas baja, no aumenta después de TSH | Baja, pero aumenta después del TSH |
| Colesterol: elevado (normalmente) | Normal (corrientemente) |
| Acido úrico: elevado en los hombres y mujeres posmenospáusicas | Igual |
| Gonodotropinas urinarias: positivas | Ausentes |
| 17- Cetosterioides: bajos | Menores |
| MB: normalmente bajo; aunque muy variable | Igual |
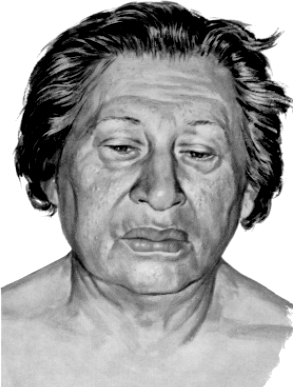
Fig. 2: Facies característica del mixedema: rasgos duros; labios gruesos; piel seca; párpados entumecidos; expresión letárgica y melancólica; pelo grueso
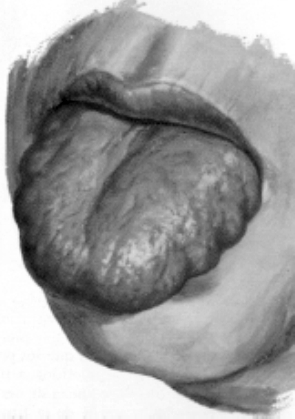
Fig. 3: Megaloglosia;
la lengua muestra impresiones dentales
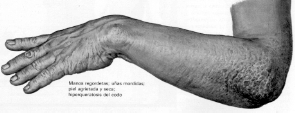
Fig. 4: Manos regordetas;
uñas mordias; piel agrietada y seca; hiperqueratosis del codo
BIBLIOGRAFIA:
Ir al
Indice General
Ir a la Tapa de la Revista
Volver a la página
de la Facultad